Elektrolýza
Protokol č.
Trieda: Meno a priezvisko: Dátum:
Téma: Elektrolýza
Úloha: Zistite rozkladné napätie Ur roztoku vody a NaCl a urobte elektrolýzu síranu meďnatého
Teoretický úvod: Elektrolýza - prebieha v elektrolyzéri, do ktorého sú ponorené dve
elektródy (katóda a anóda) na ktoré je pripojený zdroj napätia. Podstatou elektrolýzy je prechod jednosmerného elektrického prúdu roztokom alebo taveninou, pričom dochádza k pohybu iónov a ich vylúčeniu sa na elektródach. Podmienkou pre priebeh elektrolýzy je, že roztok alebo tavenina soli musí obsahovať voľne pohyblivé ióny.
Pomôcky: elektrolyzér, elektródy, zdroj jednosmerného elektrického prúdu, vodiče so svorkami na pripevnenie elektród, demonštračné meracie prístroje - avomety, destilovaná voda, NaCl.
Postup:
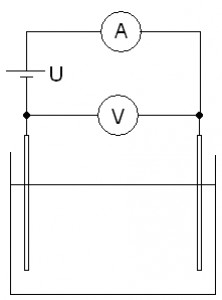
1. Do elektrolyzéra nalejeme destilovanú vodu. Zapojíme elektický obvod podľa schémy. Zvyšujeme napätie zdroja od nuly po maximum - 12 V a určíme, aký prúd tečie.
2. Do vody nasypeme NaCl. Napätie opäť zvyšujeme od nuly po maximum - 12 V.
Zistíme hodnoty U a I a zapíšeme ich do tabulky (minimáhie 5 hodnôt). Nakreslíme graf- závislosť U a I. Priesečník osi U a grafu určuje rozkladné napätie Ur.
3. Elektrolytom môže byť aj roztok síranu meďnatého (CuSO4) vo vode, kladná eletróda musí byť z medi, zápornú eletródu tvorí pokovovaný predmet.
Náčrt:
Tabuľka:
P.č. | 1. | 2. | 3. | 4. | 5. |
U[V] |
|
|
|
|
|
I[mA] |
|
|
|
|
|
Graf: I=f(I)
Záver:
1. Destilovaná voda prúd ...
2. Rozkladné napätie Ur je ...
3.CuSO4 sa vo vode disociuje na ...katióny medi Cu2+ a anióny SO42-. Ióny Cu2+ sú priťahované k zápornej elektróde, na ktorej postupne vytvárajú medený povlak. Ióny SO42- sú priťahované ku kladnej medenej elektróde, z ktorej vytrhávajú katióny medi Cu2+. Koncentrácia roztoku zostáva rovnaká, medená elektróda sa časom rozpustí - galvanizácia